Autor:
Helen Garcia
Loomise Kuupäev:
17 Aprill 2021
Värskenduse Kuupäev:
1 Juuli 2024

Sisu
- Sammud
- Meetod 1: 2: normaalsuse arvutamine molaarsuse abil
- Meetod 2/2: normaalsuse arvutamine ekvivalentses massis
- Näpunäiteid
- Mida sul vaja on
Normaalsus näitab happe või leelise kontsentratsiooni lahuses. Lahuse normaalsuse väljaselgitamiseks võib arvutustes kasutada nii molaarsust kui ka molekuli ekvivalentset massi. Kui otsustate kasutada molaarsust, kasutage valemit N = M (n), kus M on molaarsus ja n on vesiniku või hüdroksiidi molekulide arv. Kui otsustate kasutada samaväärset massi, kasutage valemit N = eq ÷ V, kus eq on ekvivalentide arv ja V on lahuse maht.
Sammud
Meetod 1: 2: normaalsuse arvutamine molaarsuse abil
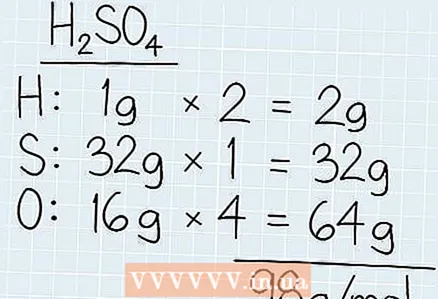 1 Lisage lahuse kõigi komponentide molaarmass. Leidke perioodilisustabelist keemilise valemi elemendid, et teada saada nende aatommass, mis vastab molaarmassile. Kirjutage üles iga elemendi molaarmass ja korrutage see nende elementide arvuga. Kogu molaarmassi leidmiseks lisage kõigi komponentide molaarmass.
1 Lisage lahuse kõigi komponentide molaarmass. Leidke perioodilisustabelist keemilise valemi elemendid, et teada saada nende aatommass, mis vastab molaarmassile. Kirjutage üles iga elemendi molaarmass ja korrutage see nende elementide arvuga. Kogu molaarmassi leidmiseks lisage kõigi komponentide molaarmass. - Näiteks kui soovite teada väävelhappe molaarmassi (H2NII4), selgitage välja vesiniku (1 g), väävli (3 g) ja hapniku (16 g) molaarmass.
- Korrutage mass kompositsiooni komponentide arvuga. Meie näites on 2 vesinikuaatomit ja 4 hapnikuaatomit. Vesiniku kogumoolmass on 2 x 1 g = 2 g. Selles lahuses on hapniku molaarmass 4 x 16 g = 64 g.
- Lisage kõik molaarmassid kokku. Saate 2 g + 32 g + 64 g = 98 g / mol.
- Kui teate juba otsitava lahuse molaarsust, minge otse 4. sammu juurde.
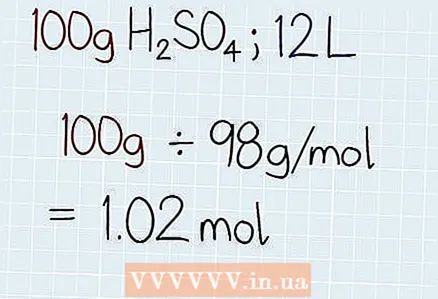 2 Jagage lahuse tegelik mass molaarmassiga. Uurige lahenduse tegelikku kaalu. See märgitakse kas lahusega mahutile või ülesandele endale.Seejärel jagage lahuse mass varem leitud kogu molaarmassiga. Tulemuseks on lahuses olevate moolide arv, mille järel tuleb kirjutada “mool”.
2 Jagage lahuse tegelik mass molaarmassiga. Uurige lahenduse tegelikku kaalu. See märgitakse kas lahusega mahutile või ülesandele endale.Seejärel jagage lahuse mass varem leitud kogu molaarmassiga. Tulemuseks on lahuses olevate moolide arv, mille järel tuleb kirjutada “mool”. - Näiteks kui proovite teada saada 100 g H normaalsust2NII4lahustatakse 12 liitris vedelikus, kasutage tegelikku massi ja jagage molaaride vahel. Selle tulemusena saate: 100 g ÷ 98 g / mol = 1,02 mol.
- 1 mool võrdub 6,02 x 10 aatomi või lahuse molekuliga.
 3 Molaarsuse väljaselgitamiseks jagage tulemus lahuse mahuga liitrites. Võtke äsja arvutatud lahuse moolide arv ja jagage see mõõdetava lahuse kogumahuga. Selle tulemusena teate molaarsust (M), mille abil saate teada lahuse kontsentratsiooni.
3 Molaarsuse väljaselgitamiseks jagage tulemus lahuse mahuga liitrites. Võtke äsja arvutatud lahuse moolide arv ja jagage see mõõdetava lahuse kogumahuga. Selle tulemusena teate molaarsust (M), mille abil saate teada lahuse kontsentratsiooni. - Meie näite põhjal saame järgmise valemi: 1,02 mol ÷ 12 L = 0,085 M.
Nõuanne: muundage kindlasti lahuse maht liitriteks, kui te pole seda veel teinud. Vastasel juhul saate vale vastuse.
 4 Korrutage molaarsus vesiniku või hüdroksiidi molekulide arvuga. Vaadake keemilist valemit, et teada saada vesiniku aatomite (H) arv happes või hüdroksiidmolekulides (OH) aluses. Seejärel korrutage lahuse molaarsus vesiniku või hüdroksiidi molekulide arvuga selles lahuses, et leida normaalne kontsentratsioon või normaalsus. Vastuse lõpus kirjutage lühend "N".
4 Korrutage molaarsus vesiniku või hüdroksiidi molekulide arvuga. Vaadake keemilist valemit, et teada saada vesiniku aatomite (H) arv happes või hüdroksiidmolekulides (OH) aluses. Seejärel korrutage lahuse molaarsus vesiniku või hüdroksiidi molekulide arvuga selles lahuses, et leida normaalne kontsentratsioon või normaalsus. Vastuse lõpus kirjutage lühend "N". - Meie näites väävelhape (H2NII4) 2 vesinikuaatomit. Seega on valem järgmine: 0,085 M x 2 = 0,17 N.
- Teises näites on naatriumhüdroksiidil (NaOH) molaarsusega 2 M ainult 1 hüdroksiidmolekul. Seetõttu on valem järgmine: 2 M x 1 = 2 N.
Meetod 2/2: normaalsuse arvutamine ekvivalentses massis
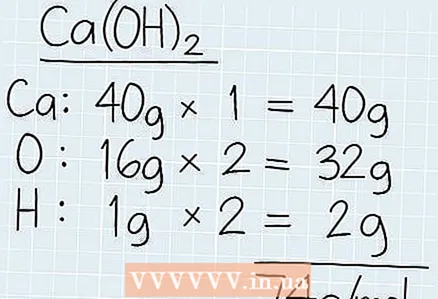 1 Uurige lahuse kogu molaarmassi. Vaadake lahuse keemilist valemit ja leidke perioodilisustabelist iga element. Kirjutage üles iga elemendi molaarmass ja korrutage see valemis olevate elementide arvuga. Liitke kõik molaarmassid kokku, et leida kogu molaarmass grammides.
1 Uurige lahuse kogu molaarmassi. Vaadake lahuse keemilist valemit ja leidke perioodilisustabelist iga element. Kirjutage üles iga elemendi molaarmass ja korrutage see valemis olevate elementide arvuga. Liitke kõik molaarmassid kokku, et leida kogu molaarmass grammides. - Näiteks kui soovite teada Ca (OH) molaarmassi2, seejärel saate teada kaltsiumi (40 g), hapniku (16 g) ja vesiniku (1 g) molaarmassi.
- Valemis on 2 hapniku ja vesiniku aatomit. Hapniku kogumass on: 2 x 16 g = 32 g. Vesiniku molaarmass on: 2 x 1 g = 2 g.
- Lisage kõik molaarmassid kokku, et saada 40 g + 32 g + 2 g = 74 g / mol.
 2 Jagage molaarmass vesiniku või hüdroksiidi molekulide arvuga. Uurige vesiniku aatomite (H) arvu happe või hüdroksiidi (OH) molekulides aluses. Jagage äsja saadud molaarmass aatomite või molekulide arvuga, et leida 1 ekvivalent, mis võrdub 1 mooli vesiniku või hüdroksiidi massiga. Vastuse lõppu kirjutage lühend "G.-e.", mis tähendab ekvivalendi massi.
2 Jagage molaarmass vesiniku või hüdroksiidi molekulide arvuga. Uurige vesiniku aatomite (H) arvu happe või hüdroksiidi (OH) molekulides aluses. Jagage äsja saadud molaarmass aatomite või molekulide arvuga, et leida 1 ekvivalent, mis võrdub 1 mooli vesiniku või hüdroksiidi massiga. Vastuse lõppu kirjutage lühend "G.-e.", mis tähendab ekvivalendi massi. - Meie näites on Ca (OH)2 2 kaks vesiniku molekuli, mis tähendab, et ekvivalendi mass on 74 g / mol ÷ 2 = 37 G.-e.
 3 Jagage lahuse tegelik kaal samaväärse massiga. Kui olete ekvivalendi massi teadnud, jagage see lahuse massiga, mis on märgitud lahusega mahutile või lahendatavale probleemile. Vastus on lahendi ekvivalentide arv, et saaksite seejärel normaalsuse arvutada. Vastuse lõppu lisage lühend "e."
3 Jagage lahuse tegelik kaal samaväärse massiga. Kui olete ekvivalendi massi teadnud, jagage see lahuse massiga, mis on märgitud lahusega mahutile või lahendatavale probleemile. Vastus on lahendi ekvivalentide arv, et saaksite seejärel normaalsuse arvutada. Vastuse lõppu lisage lühend "e." - Kui meie näites on 75 g Ca (OH)2, siis on valem järgmine: 75 g ÷ 37 G.-e = 2,027 Oe.
 4 Jagage ekvivalentide arv lahuse mahuga liitrites. Uurige välja lahuse kogumaht ja kirjutage vastus liitritesse. Normaalsuse väljaselgitamiseks võtke äsja saadud ekvivalentide arv ja jagage lahuse mahuga. Vastuse lõppu lisage lühend "N".
4 Jagage ekvivalentide arv lahuse mahuga liitrites. Uurige välja lahuse kogumaht ja kirjutage vastus liitritesse. Normaalsuse väljaselgitamiseks võtke äsja saadud ekvivalentide arv ja jagage lahuse mahuga. Vastuse lõppu lisage lühend "N". - Kui 8 liitrises lahuses on 75 g Ca (OH)2, seejärel jagage ekvivalentide arv ruumalaga järgmisel viisil: 2,027 Oe. ÷ 8 l = 0,253 N.
Näpunäiteid
- Hapete ja aluste mõõtmiseks kasutatakse tavaliselt normaalset kontsentratsiooni ehk normaalsust. Kui teil on vaja määrata mõne muu lahuse kontsentratsioon, tehakse seda tavaliselt molaarsuse mõõtmisega.
Mida sul vaja on
- Perioodilisustabel
- Kalkulaator