Autor:
Christy White
Loomise Kuupäev:
8 Mai 2021
Värskenduse Kuupäev:
1 Juuli 2024
Sisu
- Astuda
- Meetod 1/3: Esimene osa: elektronkestade mõistmine
- 2. meetod 3-st: teine osa: valentselektronide leidmine metallides, välja arvatud siirdemetallid
- Meetod 3/3: kolmas osa: valentselektronide leidmine siirdemetallides
- Näpunäited
- Vajadused
Valentselektronid asuvad elemendi väliskestas. Valentselektronide arv aatomis määrab keemilise sideme tüübi, mida see element võib moodustada. Parim viis valentselektronide arvu väljaselgitamiseks on elementide perioodilise tabeli kasutamine.
Astuda
Meetod 1/3: Esimene osa: elektronkestade mõistmine
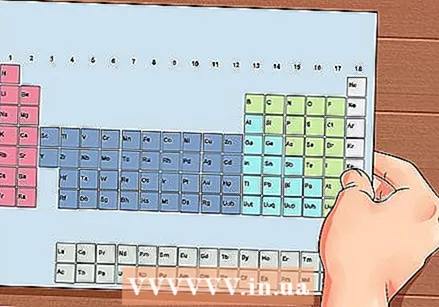 Elementide perioodiline tabel. See on värvikoodidega tabel, kus igas lahtris kuvatakse element aatominumbri ja sümbolina 1–3 tähega.
Elementide perioodiline tabel. See on värvikoodidega tabel, kus igas lahtris kuvatakse element aatominumbri ja sümbolina 1–3 tähega. 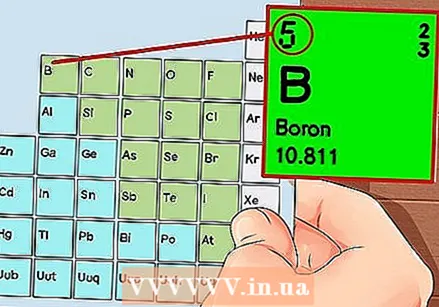 Leidke elemendi aatomnumber. Aatomnumber on elemendi sümboli kohal või kõrval. Näiteks: booril (B) on aatomnumber 5, mis tähendab, et sellel on 5 prootonit ja 5 elektroni.
Leidke elemendi aatomnumber. Aatomnumber on elemendi sümboli kohal või kõrval. Näiteks: booril (B) on aatomnumber 5, mis tähendab, et sellel on 5 prootonit ja 5 elektroni. 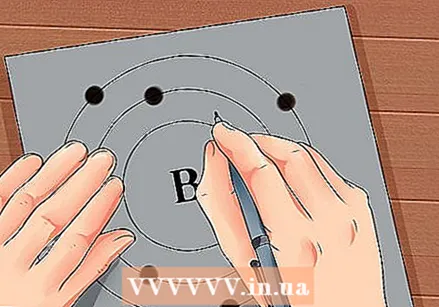 Joonistage lihtne aatomi kujutis ja asetage elektronid orbiidile tuuma ümber. Neid töökohti nimetatakse ka kestadeks või energiatasemeks. Maksimaalne elektronide arv, mis võib olla samas kestas, on fikseeritud ja kestad täidetakse sisemisest orbiidist.
Joonistage lihtne aatomi kujutis ja asetage elektronid orbiidile tuuma ümber. Neid töökohti nimetatakse ka kestadeks või energiatasemeks. Maksimaalne elektronide arv, mis võib olla samas kestas, on fikseeritud ja kestad täidetakse sisemisest orbiidist. - K kest (sisemine): maksimaalselt 2 elektroni.
- L kest: maksimaalselt 8 elektroni.
- M kest: maksimaalselt 18 elektroni.
- N kest: maksimaalselt 32 elektroni.
- O Kest: maksimaalselt 50 elektroni.
- P kest (välimine): maksimaalselt 72 elektroni.
 Leidke väliskesta elektronide arv. Need on valentselektronid.
Leidke väliskesta elektronide arv. Need on valentselektronid. - Kui valents kest on täis, on element stabiilne.
- Kui valentskest pole täis, on element reaktiivne, mis tähendab, et see võib keemiliselt siduda teise elemendi aatomiga. Iga aatom jagab oma valentselektrone, püüdes muuta valentsi kest täis.
2. meetod 3-st: teine osa: valentselektronide leidmine metallides, välja arvatud siirdemetallid
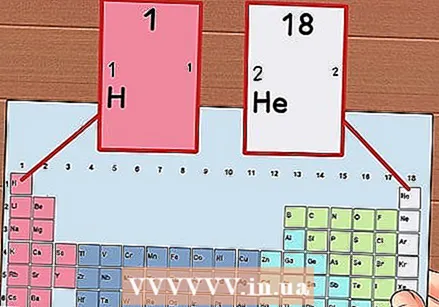 Nummerdage perioodilise tabeli iga veerg 1–18. Vesinik (H) on veeru 1 ülaosas ja heelium (ta) veeru 18. Need elemendid on erinevad rühmad.
Nummerdage perioodilise tabeli iga veerg 1–18. Vesinik (H) on veeru 1 ülaosas ja heelium (ta) veeru 18. Need elemendid on erinevad rühmad. 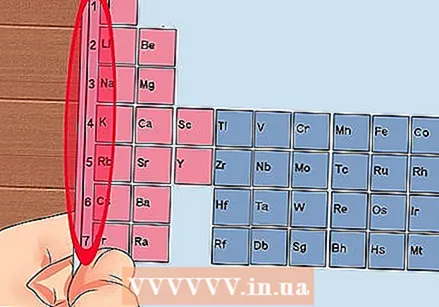 Andke igale reale arv vahemikus 1 kuni 7. Need on elementide perioodid ja need vastavad aatomi kestade arvule või energiatasemele.
Andke igale reale arv vahemikus 1 kuni 7. Need on elementide perioodid ja need vastavad aatomi kestade arvule või energiatasemele. - Vesinikul (H) ja heeliumil (He) on mõlemal 1 kest, Franciumil (Fr) aga 7.
- Lantaniidid ja aktiniidid on rühmitatud ja loetletud põhitabeli all. Kõik lantaniidid kuuluvad 6. perioodi 3. rühma ja kõik aktiniidid 7. perioodi 3. rühma.
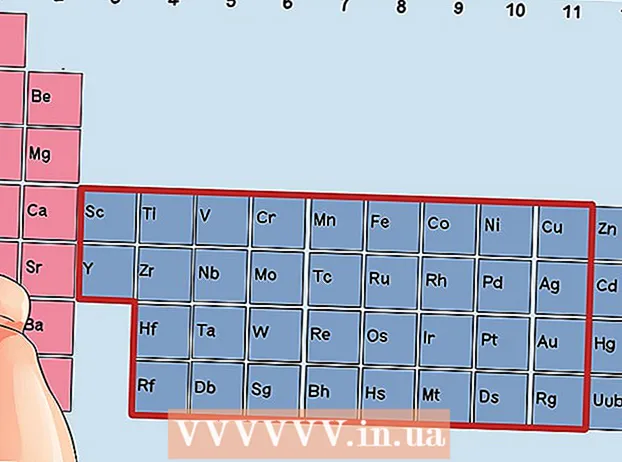
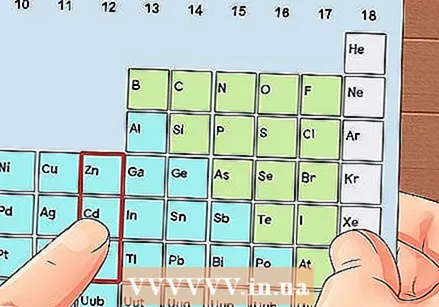 Leidke element, mis pole siirdemetall. Siirdemetallid on rühmades 3 kuni 12. Teiste metallide rühmanumbrid näitavad valentselektronide arvu.
Leidke element, mis pole siirdemetall. Siirdemetallid on rühmades 3 kuni 12. Teiste metallide rühmanumbrid näitavad valentselektronide arvu. - 1. rühm: 1 valentselektron
- 2. rühm: 2 valentselektroni
- 13. rühm: 3 valentselektroni
- Grupp 14: 4 valentselektroni
- 15. rühm: 5 valentselektroni
- Grupp 16: 6 valentselektronid
- 17. rühm: 7 valentselektroni
- 18. rühm: 8 valentselektroni - välja arvatud heelium, millel on 2
Meetod 3/3: kolmas osa: valentselektronide leidmine siirdemetallides
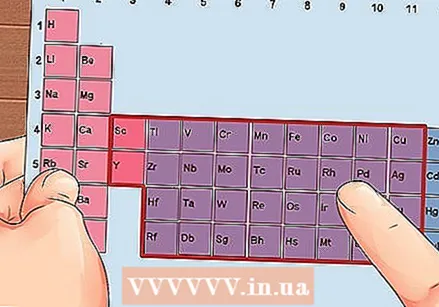 Leidke element rühmadest 3 kuni 12, siirdemetallid.
Leidke element rühmadest 3 kuni 12, siirdemetallid. Määrake valentselektronide arv rühma numbri põhjal. Need rühmanumbrid vastavad võimalikule valentselektronide arvule.
Määrake valentselektronide arv rühma numbri põhjal. Need rühmanumbrid vastavad võimalikule valentselektronide arvule. - 3. rühm: 3 valentselektroni
- 4. rühm: 2 kuni 4 valentselektroni
- 5. rühm: 2 kuni 5 valentselektroni
- 6. rühm: 2–6 valentselektroni
- 7. rühm: 2–7 valentselektroni
- 8. rühm: 2 või 3 valentselektroni
- 9. rühm: 2 või 3 valentselektroni
- 10. rühm: 2 või 3 valentselektroni
- 11. rühm: 1 või 2 valentselektroni
- 12. rühm: 2 valentselektroni
Näpunäited
- Siirdemetallidel võivad olla valentskoored, mis pole täielikult täis. Siirdemetallides valentselektronide täpse arvu kindlaksmääramiseks on vaja teatavaid kvantteooria põhimõtteid, mis jäävad väljapoole käesolevat artiklit.
Vajadused
- Elementide perioodiline tabel
- Pliiats
- Paber