Autor:
Eric Farmer
Loomise Kuupäev:
10 Märts 2021
Värskenduse Kuupäev:
1 Juuli 2024

Sisu
- Sammud
- Meetod 1: 2: neutronite arvu määramine aatomites (mitte isotoopides)
- Meetod 2/2: neutronite arvu määramine isotoopides
- Näpunäiteid
Sama elemendi aatomites on prootonite arv konstant, samas kui neutronite arv võib varieeruda.Teades, kui palju neutrone konkreetne aatom sisaldab, saate kindlaks teha, kas see on tavaline aatom või isotoop, millel on vähem või rohkem neutroneid. Neutronite arvu määramine aatomis on üsna lihtne. Aatomis või isotoobis neutronite arvu arvutamiseks on vaja ainult järgida meie juhiseid ja hoida perioodiline tabel käepärast.
Sammud
Meetod 1: 2: neutronite arvu määramine aatomites (mitte isotoopides)
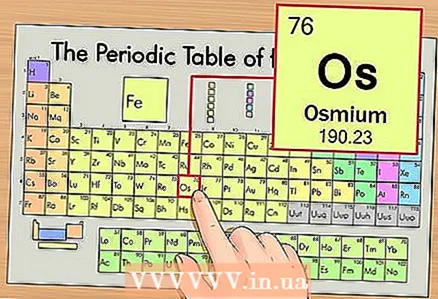 1 Leidke perioodilisustabelist element. Näitena käsitleme osmiumi (Os), mis on kuuendal perioodil (kuues rida ülevalt).
1 Leidke perioodilisustabelist element. Näitena käsitleme osmiumi (Os), mis on kuuendal perioodil (kuues rida ülevalt).  2 Leidke elemendi aatomnumber. See on reeglina elemendi lahtris kõige märgatavam number ja asub tavaliselt selle sümboli kohal (perioodilisustabeli versioonis, mida meie näites kasutame, pole muid numbreid). Aatomnumber on prootonite arv selle elemendi ühes aatomis. Osmiumi puhul on see arv 76, see tähendab, et ühes osmiumi aatomis on 76 prootonit.
2 Leidke elemendi aatomnumber. See on reeglina elemendi lahtris kõige märgatavam number ja asub tavaliselt selle sümboli kohal (perioodilisustabeli versioonis, mida meie näites kasutame, pole muid numbreid). Aatomnumber on prootonite arv selle elemendi ühes aatomis. Osmiumi puhul on see arv 76, see tähendab, et ühes osmiumi aatomis on 76 prootonit. - Prootonite arv on muutumatu ja see muudab elemendi elemendiks.
 3 Leidke elemendi aatommass. See number on tavaliselt elemendi sümboli all. Pange tähele, et meie näite perioodilise tabeli versioonis pole aatommassi antud (see pole alati nii; perioodilise tabeli paljudes versioonides on aatommass märgitud). Osmiumi aatommass on 190,23.
3 Leidke elemendi aatommass. See number on tavaliselt elemendi sümboli all. Pange tähele, et meie näite perioodilise tabeli versioonis pole aatommassi antud (see pole alati nii; perioodilise tabeli paljudes versioonides on aatommass märgitud). Osmiumi aatommass on 190,23.  4 Ümardage aatommass täisarvuni. Meie näites on 190,23 ümardatud 190 -ni.
4 Ümardage aatommass täisarvuni. Meie näites on 190,23 ümardatud 190 -ni. - Aatommass on konkreetse elemendi isotoopide keskmine arv, tavaliselt ei väljendata seda täisarvuna.
 5 Lahutage aatommassist aatomnumber. Kuna prootonid ja neutronid moodustavad aatommassi absoluutse osa, siis lahutades aatomi massist prootonite arvu (st aatomnumbri, mis võrdub prootonite arvuga), saab neutronite arvu aatomis. Kümnendkoha järel olevad numbrid viitavad aatomi elektronide väga väikesele massile. Meie näites: 190 (aatommass) - 76 (prootonite arv) = 114 (neutronite arv).
5 Lahutage aatommassist aatomnumber. Kuna prootonid ja neutronid moodustavad aatommassi absoluutse osa, siis lahutades aatomi massist prootonite arvu (st aatomnumbri, mis võrdub prootonite arvuga), saab neutronite arvu aatomis. Kümnendkoha järel olevad numbrid viitavad aatomi elektronide väga väikesele massile. Meie näites: 190 (aatommass) - 76 (prootonite arv) = 114 (neutronite arv). 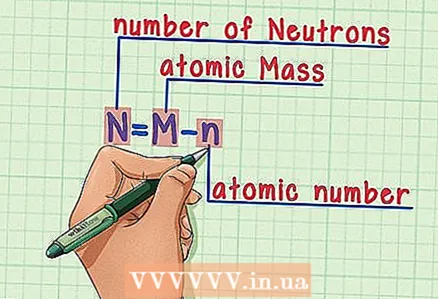 6 Pidage valemit meeles. Tulevikus neutronite arvu leidmiseks kasutage lihtsalt seda valemit:
6 Pidage valemit meeles. Tulevikus neutronite arvu leidmiseks kasutage lihtsalt seda valemit: - N = M - n
- N = neutronite arv
- M = aatommass
- n = aatomnumber
- N = M - n
Meetod 2/2: neutronite arvu määramine isotoopides
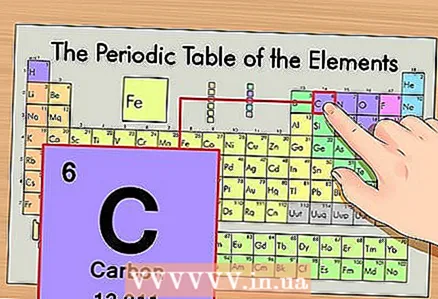 1 Leidke perioodilisustabelist element. Näitena käsitleme süsiniku 14C isotoopi. Kuna mitteisotoopne süsinik 14C on lihtsalt süsinik C, leidke süsinik perioodilisustabelist (teine periood või teine rida ülevalt).
1 Leidke perioodilisustabelist element. Näitena käsitleme süsiniku 14C isotoopi. Kuna mitteisotoopne süsinik 14C on lihtsalt süsinik C, leidke süsinik perioodilisustabelist (teine periood või teine rida ülevalt). 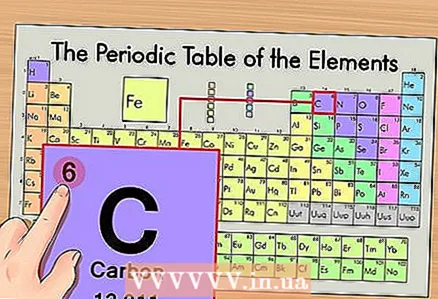 2 Leidke elemendi aatomnumber. See on reeglina elemendi lahtris kõige märgatavam number ja asub tavaliselt selle sümboli kohal (perioodilisustabeli versioonis, mida meie näites kasutame, pole muid numbreid). Aatomnumber on selle elemendi ühe aatomi prootonite arv. Süsinik on number 6, mis tähendab, et ühel süsinikul on kuus prootonit.
2 Leidke elemendi aatomnumber. See on reeglina elemendi lahtris kõige märgatavam number ja asub tavaliselt selle sümboli kohal (perioodilisustabeli versioonis, mida meie näites kasutame, pole muid numbreid). Aatomnumber on selle elemendi ühe aatomi prootonite arv. Süsinik on number 6, mis tähendab, et ühel süsinikul on kuus prootonit. 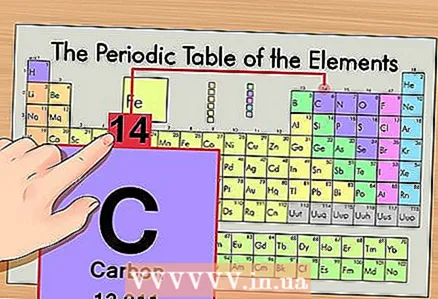 3 Leidke aatommass. Isotoopide puhul on seda väga lihtne teha, kuna neid nimetatakse nende aatommassi järgi. Meie puhul on süsiniku 14C aatommass 14. Nüüd teame isotoobi aatommassi; järgnev arvutusprotsess on sama mis neutronite arvu määramisel aatomites (mitte isotoopides).
3 Leidke aatommass. Isotoopide puhul on seda väga lihtne teha, kuna neid nimetatakse nende aatommassi järgi. Meie puhul on süsiniku 14C aatommass 14. Nüüd teame isotoobi aatommassi; järgnev arvutusprotsess on sama mis neutronite arvu määramisel aatomites (mitte isotoopides).  4 Lahutage aatommassist aatomnumber. Kuna prootonid ja neutronid moodustavad aatommassi absoluutse osa, siis lahutades aatomi massist prootonite arvu (st aatomnumbri, mis võrdub prootonite arvuga), saab neutronite arvu aatomis. Meie näites: 14 (aatommass) - 6 (prootonite arv) = 8 (neutronite arv).
4 Lahutage aatommassist aatomnumber. Kuna prootonid ja neutronid moodustavad aatommassi absoluutse osa, siis lahutades aatomi massist prootonite arvu (st aatomnumbri, mis võrdub prootonite arvuga), saab neutronite arvu aatomis. Meie näites: 14 (aatommass) - 6 (prootonite arv) = 8 (neutronite arv). 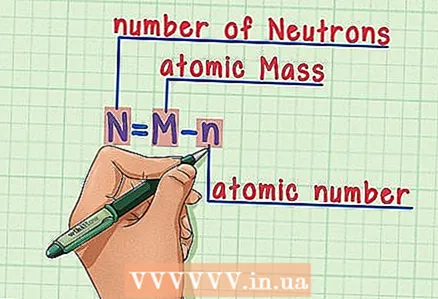 5 Pidage valemit meeles. Tulevikus neutronite arvu leidmiseks kasutage lihtsalt seda valemit:
5 Pidage valemit meeles. Tulevikus neutronite arvu leidmiseks kasutage lihtsalt seda valemit: - N = M - n
- N = neutronite arv
- M = aatommass
- n = aatomnumber
- N = M - n
Näpunäiteid
- Prootonid ja neutronid moodustavad peaaegu elementide absoluutse massi, elektronid ja muud osakesed aga äärmiselt ebaolulise massi (see mass kipub nulli).Kuna ühel prootonil on umbes sama mass kui ühel neutronil ja aatomnumber on prootonite arv, saate kogu massist lihtsalt prootonite arvu lahutada.
- Osmium - toatemperatuuril tahkes olekus metall, sai oma nime kreekakeelsest sõnast "osme" - lõhn.
- Kui te pole kindel, mida perioodilisustabeli number tähendab, pidage meeles: tabel on tavaliselt üles ehitatud aatomnumbri (st prootonite arvu) ümber, mis algab 1 -st (vesinik) ja kasvab ühe ühiku vasakult paremale , lõpetades 118 -ga (Oganesson). Seda seetõttu, et aatomi prootonite arv määrab elemendi enda ja selline arv on lihtsaim viis elementide korraldamiseks (näiteks kahe prootoniga aatom on alati heelium, nagu 79 prootoniga aatom on alati kuld ).